LPA- современный подход к реконструкции рогового слоя
Введение
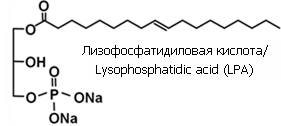
LPA (Лизофосфатидиловая кислота) -это продукт ферментного расщепления соевого лецитина, содержащий высокую концентрацию (20-30%) Лизофосфатидиловой кислоты в стабильной форме. Лизофосфатидиловая кислота естественным образом вырабатывается в организме человека и стимулирует рост, дифференциацию выживание и подвижность различных типов клеток, воздействуя на мембранные рецепторы.
С точки зрения применения в косметических средствах представляют интерес три основных ее функции:
1. Стимулирование выработки липидов и компонентов NMF в коже: церамидов и филлагрина.
2. Укрепление плотных межклеточных контактов.
3. Усиление клеточной дифференциации путём стимуляции притока Ca2+
Изменения в эпидермисе человека с возрастом
Хорошо известно, что кожный барьер - это важная функция сохранения жизни человека. Также известно, что кожный барьер истончается с возрастом из-за уменьшения уровня натурального увлажняющего фактора и межклеточных липидов, включая церамиды. Основной признак состарившейся кожи - это сухость, а корнеоциты накапливаются из-за снижения скорости обновления. Гистологически при фотостарении и в результате естественных возрастных изменений в коже также наблюдается атрофия эпидермиса. Совершенно очевидно, что нарушение барьера кожи является важной причиной ее сенсибилизации и аллергических реакций, и вызвано оно расстройствами клеточной дифференциации эпидермиса. Поэтому нормализация клеточной дифференциации эпидермиса является эффективной стратегией улучшения состояния кожного барьера. Поддержание в норме барьерных функций кожи будет препятствовать старению кожи и снизит чувствительность или аллергическую реакцию кожи.
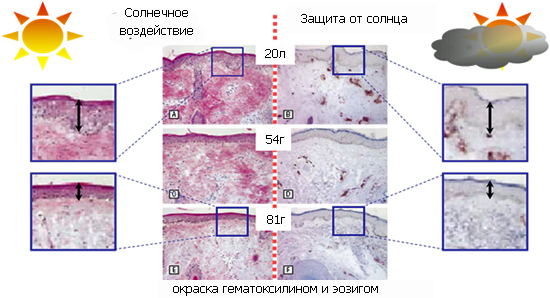
Рис. Ухудшение состояния эпидермиса в зависимости от возраста
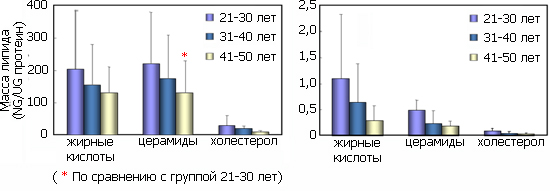
Рис. Уменьшение содержания липидов в коже на лице и руках в зависимости от возраста
Стимулированипе выработки липидов и компонентов NMF в коже: церамидов и филлагрина.
Воздействие LPA на экспрессию мРНК серинпальмитоилтрансферазы (SPT) и синтез филаггрина.
За функцию кожного барьера отвечают церамиды и межклеточные липиды, с одной стороны. Серинпальмитоилтрансфераза (SPT) - фермент, принимающий участие в синтезе эпидермальных церамидов. С другой стороны - это натуральный увлажняющий фактор, играющий важную роль в поддержании здорового состояния эпидермиса. Он состоит из свободных аминокислот, молочной кислоты, мочевины и некоторых ионов металлов. Филаггрин - предшественник свободных аминокислот в NMF.
Влияние лизофосфатидиловой кислоты на экспрессию мРНК серинпальмитоилтрансферазы и филаггрина исследовали методом полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). Клетки обрабатывались LPA в течение 12 и 24 часов в субкультурах с низкой плотностью, отобранных от сливных культур. После очистки суммарной РНК выполнили анализ ОТ-ПЦР с целью обнаружения экспрессии гена в клетках, обработанных LPA и в необработанных клетках. В качестве внутреннего контроля определили мРНК циклофилина. Лизофосфатидиловая кислота значительно увеличивала экспрессию мРНК серинпальмитоилтрансферазы и филаггрина в течение 12 часов культивирования, и это увеличение наблюдалось в течение 24 часов после обработки.
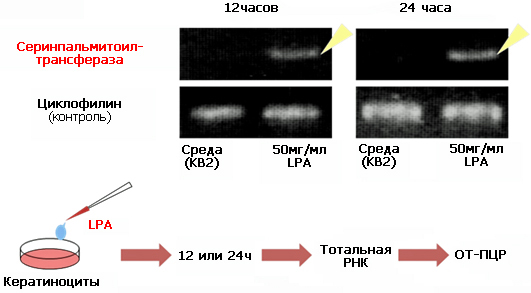
Рис. LPA стимулирует экспрессию мРНК филаггрина и серинпальмитоилтрансферазы в нормальных человеческих эпидермальных кератиноцитах.

Рис. LPA усиливает синтез мРНК филаггрина в нормальных человеческих эпидермальных кератиноцитах
Эффект лизофосфатидиловой кислоты на синтез церамидов на трехмерной модели кожи.
Для характеристики фармакологического и космецевтического воздействия исследовали влияние LPA на синтез липидов (церамидов) с помощью трехмерной модели кожи (SEM). Местное применение LPA выявило дозозависимое увеличение церамида 2. Кроме того, испытанная максимальная концентрация LPA (1 мг/мл) вызвала образование нового липида, который предварительно идентифицировали как церамид 4 или 5 на основе его изменчивости. Таким образом, было подтверждено, что лизофосфатидиловая кислота увеличивает синтез конечных структур, церамидов.
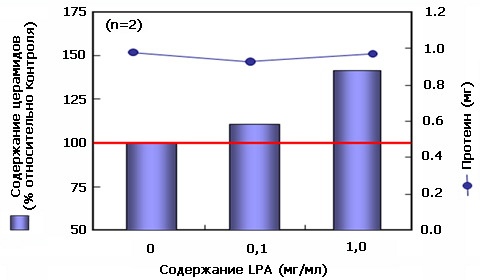
Рис. Содержание церамидов в эпидермисе модели кожи после 1 недели применения на поверхности кожи (ex-vivo).
Влияние LPA на укрепление плотных межклеточных соединений
Плотные межклеточные контакты представляет из себя плотно соединённые друг с другом мембраны клеток, которые формируют своеобразный барьер, удерживающий влагу в коже. Их состав формируется протеинами клаудином и окклюдином, объединяя цитоскелеты соседних клеток.
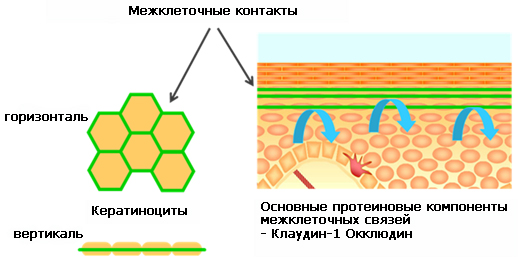
Межклеточные связи выполняют различные жизненно важные функции. Во-первых, они удерживают клетки вместе, формируя плотный клеточный матрикс. Эти плотные контакты блокируют движение интегральных мембранных белков между апикальной и базолатеральной поверхностями клетки, что позволяет дифференцировать функции каждой поверхности клетки (например, рецептор- опосредованный эндоцитоз на апикальной поверхности и экзоцитоз на базолатеральной поверхности) , что поддерживает трансцеллюлярный транспорт веществ.
Плотные межклеточные связи препятствуют просачиванию молекул и ионов в межклеточное пространство, благодаря чему питательные вещества попадают непосредственно внутрь клетки (посредством диффузии или активного транспорта). Последние исследования показывают, что состояние плотных связей связано с внеклеточным содержанием липидов (увлажнённостью кожи).
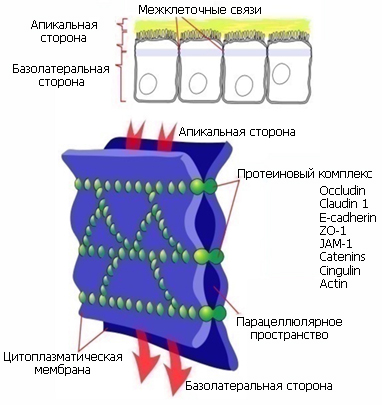
Функции плотных межклеточных соединений:
1. Барьерные функции: поддержание необходимого содержания влаги и липидов в эпидермисе.
2. Контроль процесса кератинизации в эпидермисе (предотвращение элюирования ионов из эпидермиса).
3. Регулирование липидного обмена (Стимуляция синтеза и высвобождения липидов в эпидермисе).
LPA усиливает экспрессию протеинов Клаудин-1 и Окклюдин- главных составляющих плотных межклеточных связей.
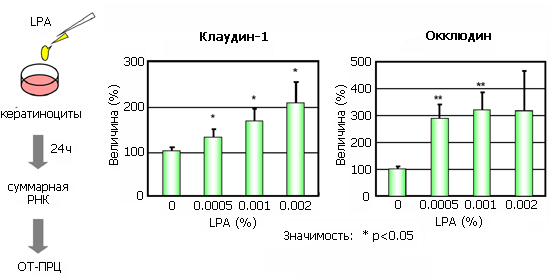
Рис. Усиление экспрессии генов Клаудина-1 и Окклюдина при применении LPA.
В исследовании с использованием нормальных кератиноцитов человека оценивалось влияние LPA на синтез основных протеинов межклеточных плотных связей - Окклюдина и Клаудина-1. Количество этих протеинов определяли методом иммунного окрашивания. При использовании LPA в концентрации 10 мг/мл наблюдалось значительное увеличение синтеза Окклюдина и Клаудина-1.
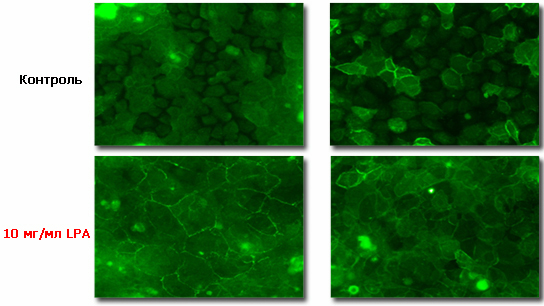
Рис. Микроснимок кератиноцитов человека до и после использования LPA
В составе плотных межклеточных контактов присутствуют также и другие функционально важные белки, взаимодействие которых обеспечивает должный парацеллюлярный перенос веществ и барьерные функции эпидермиса. Это белки так называемой "зоны склеивания"/ zonnula occludens, в частности белки ZO-1 и ZO-2 (см. рис.ниже)
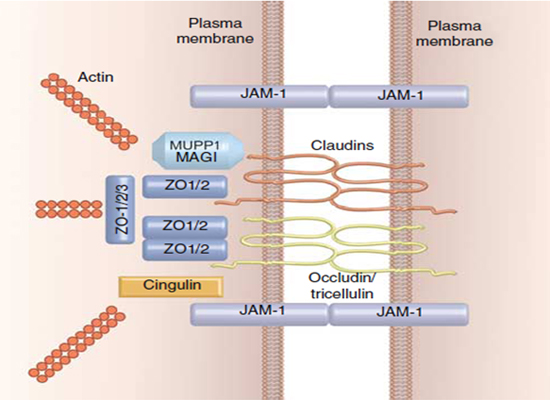
Рис. Белки в составе плотных межклеточных контактов
LPA повышает экспрессию гена белков Zonula Occludens (ZO-1 и ZO-2).

Рис. Увеличение экспрессии белков ZO-1 и ZO-2 при использовании LPA
LPA стимулирует дифференциацию клеток, способствуя уменьшению размера пор и поддержанию здорового состояния эпидермиса.
cДифференциация клеток- процесс, в результате которого менее специализированные клетки становятся более специализированными для выполнения своих функций. В коже при дифференциации клетки медленно перемещаются вверх через эпидермис в роговой слой, где клетки, уже без ядра, постоянно отслаиваются с поверхности кожи (десквамация). Одним из основных стимуляторов дифференциации клеток в эпидермисе являются ионы кальция , получаемые клетками из внутриклеточного пространства.Наиболее важная функция эпидермиса человека- это создание и сохранение эффективных барьерных функций, позволяющих свести к минимуму трансэпидермальную потерю воды и защитить от обезвоживания. Кроме того, кожа обеспечивает естественный барьер против проникновения экзогенных веществ.
Эти барьерные функции достигаются путем сложного процесса дифференциации клеток эпидермиса, которые развиваются из митотически активных базальных клеток в мертвые, плоские чешуйки рогового слоя, плотно связанные друг с другом и окруженные липидными слоями. В процессе дифференциации базальные кератиноциты отделяются от базальной мембраны, пролиферация замедляется, в кератиноцитах синтезируются структурные белки и энзимы. Между клетками образуется межклеточное цементирующее вещество, содержащее липиды и непроницаемое для воды. В результате образуется непроницаемый протеиново- липидный барьер, который и защищает нас.
Дифференциация кератиноцитов существенно регулируется внутриклеточным Ca2+, который, в свою очередь, влияет на несколько путей сигнальной трансдукции. Проведенные исследования указывают на то, что лизофосфатидиловая кислота увеличивает уровень внутриклеточного Ca2+ посредством возбуждения канала Ca2+ L-типа. Сигнал активизирует PKCα и пути кальмодулина и в итоге ускоряет клеточную дифференциацию эпидермиса. LPA ускоряет поглощение клетками ионов Ca2+ , что проявляется в немедленном воздействии на процесс дифференциации.
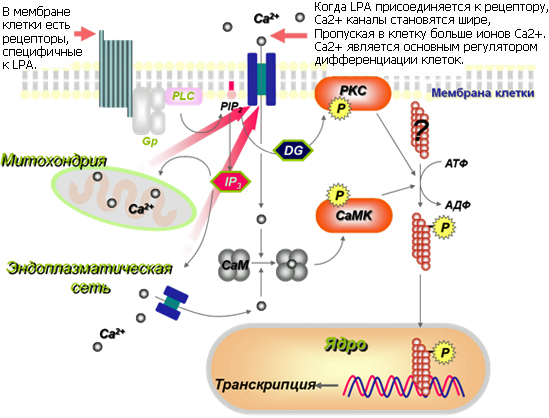
Рис. Механизм воздействия LPA на приток Ca2+ в клетку
Воздействие LPA на поступление Ca2+ в клетку
Исследовалось влияние лизофосфатидиловой кислоты на уровень внутриклеточного Ca2+ . Кератиноциты культивировали с несколькими растворами лизофосфатидиловой кислоты в разной концентрации в питательной среде с Ca2+ (с=0,03 ммоль) или без него в течение 1 часа. После удаления питательной среды количество ионов Ca2+ в клетке определили с использованием Fura-2/AM. Как показано на рис. 10, количество внутриклеточного Ca2+ увеличилось после культивирования в питательной среде, содержащей LPA и Ca2+, однако увеличение уровня Ca2+ не наблюдалось в отсутствие Ca2+. Эти результаты указывают на то, что лизофосфатидиловая кислота ускоряет поступление Ca2+ из внеклеточной среды за счет активации кальциевых каналов.
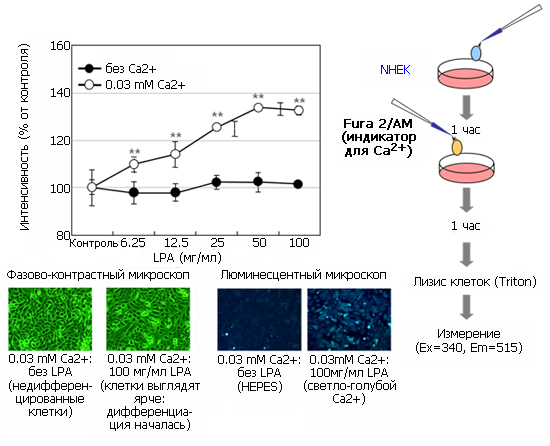
Рис. LPA влияет на инфлюкс Ca2+ в нормальных человеческих кератиноцитах эпидермиса
Влияние LPA на фосфорилирование PKCα
Протеинкиназа С альфа (PKCα) -фермент, играющий важную роль в передаче сигнала от клетки к клетке, регуляции дифференцировки и роста клеток. Это кальций зависимый фермент, т.е. для его полной активации необходимо участие Ca2+.
Чтобы выяснить влияние LPA на систему сигнальной трансдукции исследовали уровни фосфорилирования PKCa в кератиноцитах после применения лизофосфатидиловой кислоты. Протеинкиназа PKCα была фосфорилирована в кератиноцитах, обработанных LPA.
Кератиноциты, обработанные LPA, собрали после следующих временных отрезков экспозиции: 0,5, 1 и 2 часа. После сбора лизатов измерили концентрации белка и после применения такого же количества белка отделили их посредством электрофореза в геле. Фосфорилированную PKCα определяли методом иммуноблоттинга с использованием специфических антител. Как показано на рисунке ниже, фосфорилирование PKCα немедленно увеличилось после применения LPA и продолжало увеличиваться в течение 2 часов после ее применения с временной зависимостью.
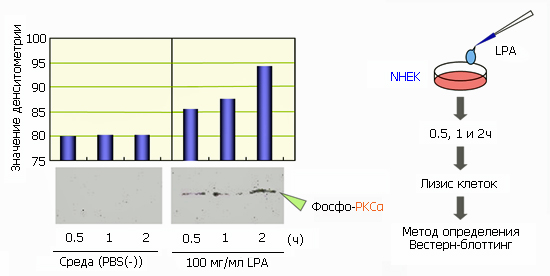
Рис. Влияние LPA на фосфорилирование PKCα.
Тесты in-vivo. Улучшение состояния рогового слоя
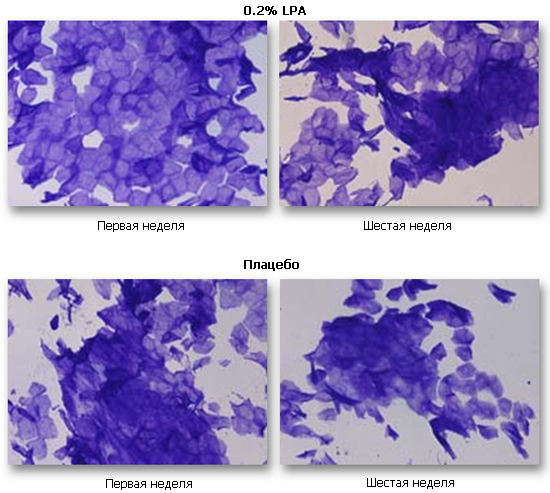
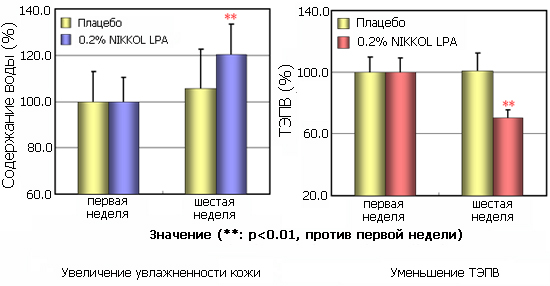
На микроснимках видно, что после использования 0.2% LPA состояние рогового слоя улучшилось: корнеоциты упакованы тонким слоем, имеют гексагональную форму, не наблюдается нуклеированных клеток, т.е. роговой слой находится в очень хорошем состоянии. Благодаря укреплению рогового слоя, наблюдается снижение уровня трансэпидермальной потери воды и, как следствие, увеличение содержания влаги в коже (см. диаграммы ниже). В то же время, при использовании плацебо изменений не наблюдается.
Влияние LPA на размер пор. Взаимосвязь между барьером кожи и размером пор
Расширенные поры - одна из распространенных проблем , вызывающих беспокойство у женщин разного возраста.
При исследовании таких пор было выявлено присутствие в роговом слое клеток, содержащих ядра, признак паракератоза (рис. 12). Изучая зависимость между степенью выраженности пор и состоянием рогового слоя ученые выявили, что у женщин, кожа которых отличается расширенными порами, очень высокий уровень потери влаги (ТЭПВ) в эпидермисе. (Life Science Research Center, Shiseido).
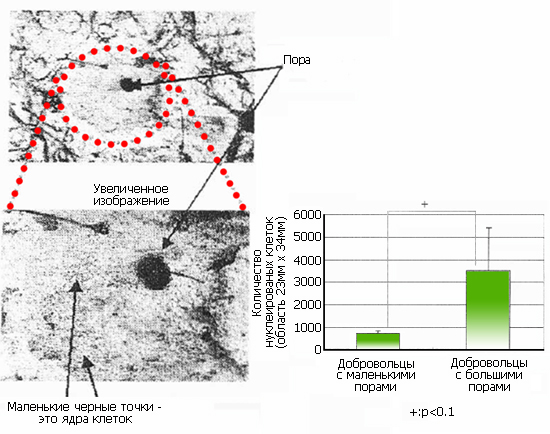
Рис. Присутствие нуклеированых клеток (паракератоз) вокруг пор (на щеках). Life Science Research Center, Shiseido. Fragrance Journal №3, 2004.
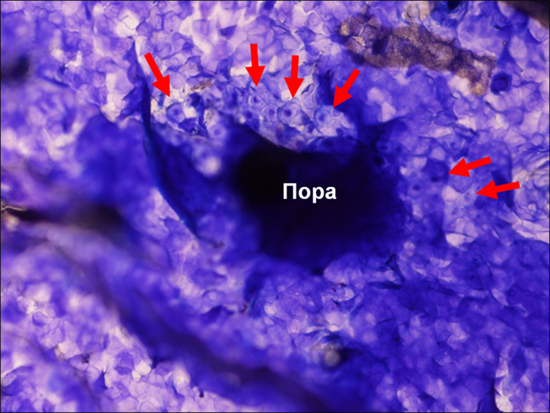
Рис. Наличие нуклеированых клеток (паракератоз) вокруг пор (кожа щек).
В исследованиях изучалос ь влияние LPA на размер пор. В эксперименте принимали участие 11 добровольцев. Крем с 0.1% LPA наносили на кожу лица дважды в день в течение 4 недель. Было доказано, что 0.1 % LPA сокращает размер и количество пор на 20%.
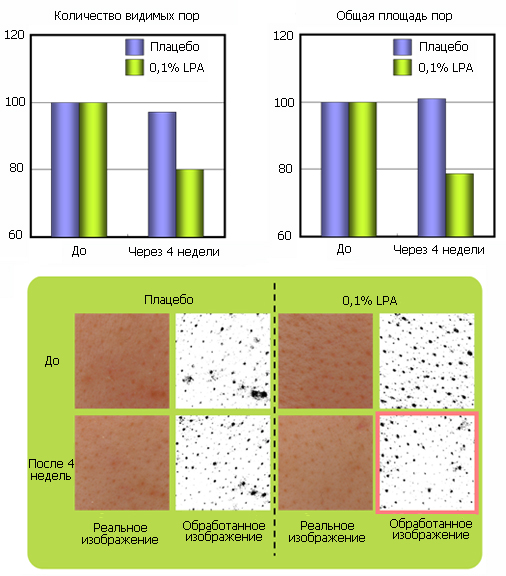
Образец: 0,05% LPA лосьон и Плацебо лосьон
Группа: 8 волонтеров
Период: 4 недели
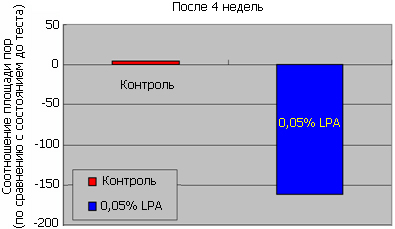
Вывод: наблюдалось статистически значимое и визуально определяемое уменьшение размера пор.
Средний размер пор сократился на 8.5% в течении 4 недель.
Улучшение тона кожи при использовании 0.1 % LPA
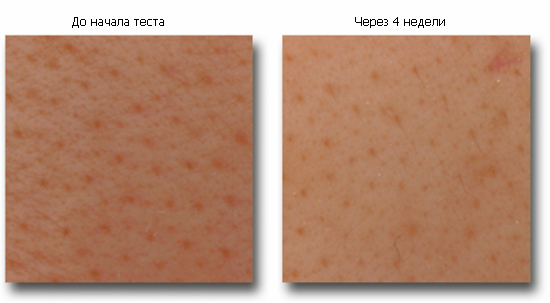
Рис. Использование 0.1 % LPA в течение 4 недель заметно улучшает / осветляет тон кожи.
Cвойства LPA
РастворимостьLPA растворима в воде и глицерине. Однако, не растворима в этаноле, маслах и полиолах, кроме глицерина.
| Ингредиент | Концентрация (wt%) | ||||
| 0.1 | 0.2 | 0.5 | 1.0 | 10.0 | |
| Вода | ◊ | ◊ | ◊ | ◊ | □ |
| Глицерин | ■ | ■ | ■ | ■ | ■ |
| Этанол | □ | □ | □ | □ | □ |
| 1,3-БГ | □ | □ | □ | □ | □ |
■ Растворим □ Не растворим ◊ Прозрачный
Растворимость 1% водного раствора LPA в растворе этанола.
| Концентрация этанола (wt%) в растворе | 5 | 10 | 20 |
| Результат наблюдений | Слегка мутный | Слегка мутный | Не растворим |
Рекомендуемый уровень pH: LPA стабильна при pH 6-8
Стабильность LPA
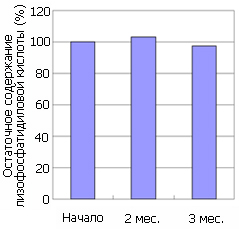
Cтабильность LPA оценивали с помощью теста на ускоренное старение. LPA помещали в темное место в течение 3 месяцев при температуре 45оC, и затем измеряли содержание лизофосфатидиловой кислоты через 2 и 3 месяца. Содержание лизофосфатидиловой кислоты в LPA практически не изменилось по сравнению с исходным значением. Кроме этого, пероксидное чило было менее 1.0 meq/kg после окончания этого теста, что говорит о высокой устойчивости к окислению LPA.
В присутствии ионов металлов рекомендуется использование хелатирующих агентов.
Стабильность в готовых рецептурах
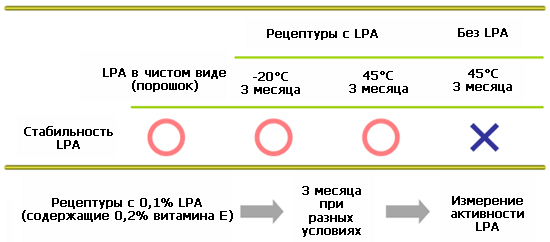
Информация об ингредиенте
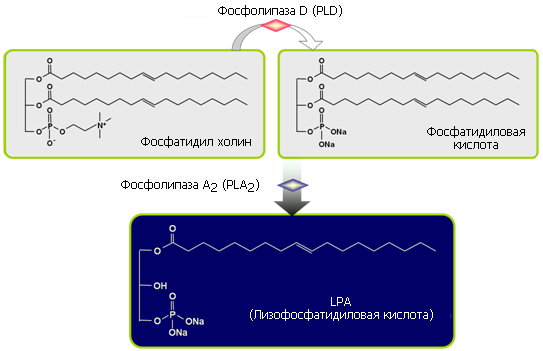
В синтезе LPA используется особый запатентованный метод для стабилизации молекулы. Ферменты, используемые в синтезе - не животного происхождения. Используются ферменты, вырабатываемые микроорганизмами.
| INCI Name: | Lysophosphatidic acid, Lecithin, Lysolecithin |
| Антиоксидант: | d-дельта-токоферол (0.2%) |
| Внешний вид: | Белый или желтоватый порошок |
| Состав: | Лизофосфатидиловая кислота (содержание: 20-30%)Лецитин (30-40%); Лизолецитин (менее 10%). |
| Безопасность | |
| Токсичность | Отрицательно (3T3-NR метод) |
| Раздражение слизистой глаз | Отрицательно (SIRC-NR метод) |
| Первичное раздражение кожи | Отрицательно (накожный тест; 2% водный р-р, 24 ч) |
| Мутагенность | Отрицательно (AMES) |